Notre travail traite de l’impressionnante capacité des bactéries à acquérir et à échanger des gènes… qui leur permettent d’évoluer de manière très rapide et efficace !
Nous étudions les mécanismes responsables de la variabilité du génome bactérien avec un intérêt tout particulier pour ceux qui sont impliqués dans l’acquisition de gènes exogènes (transfert horizontal de gènes). Notre système-modèle est l’intégron, un système naturel de capture et d’expression de gènes impliqué dans le développement et la dissémination de gènes de résistance aux antibiotiques, principalement parmi les bactéries à Gram négatif. Nous caractérisons les mécanismes moléculaires de la recombinaison dans ces éléments génétiques, ainsi que leur évolution et leur impact phénotypique sur la physiologie des cellules bactériennes qui les hébergent.
Récemment nous avons entrepris l’étude des effets de concentrations sub-inhibitrices d’antibiotiques sur l’induction de la réponse SOS bactérienne, et sur leur rôle en tant que déclencheurs de stress. Nous utilisons principalement des approches génétiques et post-génomiques pour aborder ces questions.
Notre équipe étudie également les facteurs jouant un rôle dans la réparation et la maintenance des deux chromosomes de Vibrio cholerae. Toutes les espèces appartenant au genre Vibrio possèdent un génome constitué de deux chromosomes circulaires ayant des caractéristiques dynamiques distinctes, et nous cherchons à comprendre l’avantage sélectif de cette structuration, ainsi que le mécanisme spécifique chargé de coordonner la réplication des deux chromosomes.
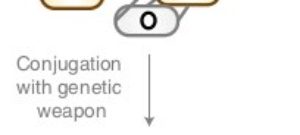
Nous avons récemment développé une nouvelle technologie antimicrobienne, basée sur l’expression et la livraison de modules toxines-intéines qui sont exclusivement activés dans les bactéries pathogènes résistantes aux antibiotiques ciblées.
Une explication de notre article publié récemment dans Nature Biotechnology