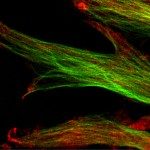
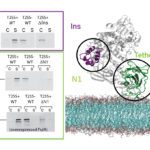
L’équipe Systèmes macromoléculaires s’intéresse aux mécanismes moléculaires qui gouvernent le transport des protéines et la biogenèse des organelles chez les bactéries à Gram négatif. En étudiant Escherichia coli et Klebsiella comme modèles, nous sommes focalisés sur le système de sécrétion de type II et sur l’assemblage de filaments de surface de la famille des pili de type IV. Ces deux nanomachines complexes partagent des composants protéiques et mécanismes similaires. Les deux systèmes catalysent l’assemblage des filaments flexibles à partir de sous-unités protéiques initialement enchâssées dans la membrane interne. Dans le système de sécrétion de type II, ces filaments (appelés endopili) favorisent la sécrétion de protéines entièrement repliées du périplasme à travers la membrane externe. Les pili de type IV chez Escherichia coli sont impliqués dans l’adhésion bactérienne aux surfaces et motilité. Ces pili sont co-régulés avec les gènes de compétence naturelle et probablement jouent un rôle dans la transformation. Depuis cette année, nous sommes impliqués dans deux projets collaboratifs, financés par l’ANR-NSF et par le HFSP. Dans ce cadre, notre objectif est de disséquer les mécanismes de sécrétion et d’assemblage des nanocables chez les bactéries du sol telles que Geobacter. Ces nanocables permettent le transfert d’électrons a distance directement d’un microorganisme à l’autre en anaérobie et leur biogenèse repose sur des versions encore inexplorées des systèmes d’assemblage de filaments de type IV.
Nous intégrons des analyses génétiques, biochimiques et fonctionnelles avec des approches structurelles, biophysiques et de modélisation pour comprendre en détails les systèmes macromoléculaires dynamiques l’enveloppe bactérienne. Les études mécanistiques de ces systèmes sont étroitement liées à des questions plus fondamentales sur les interactions protéine-protéine et protéine-membrane, le rôle des ions, le repliement des protéines, leur localisation, contrôle de qualité et stabilité.