Lien vers Pubmed [PMID] – 30561149
Lien DOI – 10.1111/mmi.14188
Mol Microbiol 2019 Mar; 111(3): 732-749
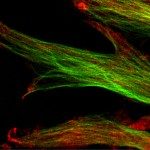
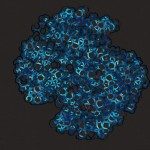
Type 4a pili (T4aP) are long, thin and dynamic fibres displayed on the surface of diverse bacteria promoting adherence, motility and transport functions. Genomes of many Enterobacteriaceae contain conserved gene clusters encoding putative T4aP assembly systems. However, their expression has been observed only in few strains including Enterohaemorrhagic Escherichia coli (EHEC) and their inducers remain unknown. Here we used EHEC genomic DNA as a template to amplify and assemble an artificial operon composed of four gene clusters encoding 13 pilus assembly proteins. Controlled expressions of this operon in nonpathogenic E. coli strains led to efficient assembly of T4aP composed of the major pilin PpdD, as shown by shearing assays and immunofluorescence microscopy. When compared with PpdD pili assembled in a heterologous Klebsiella T2SS type 2 secretion system (T2SS) by using cryo-electron microscopy (cryoEM), these pili showed indistinguishable helical parameters, emphasizing that major pilins are the principal determinants of the fibre structure. Bacterial two-hybrid analysis identified several interactions of PpdD with T4aP assembly proteins, and with components of the T2SS that allow for heterologous fibre assembly. These studies lay ground for further characterization of the T4aP structure, function and biogenesis in enterobacteria.