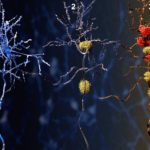
La cochlée, appareil sensoriel auditif des mammifères, est l’organe où a lieu la première étape de la perception des sons, au cours de laquelle un son complexe incident est détecté et décomposé suivant sa fréquence fondamentale et ses fréquences harmoniques. Cette analyse fréquentielle (dite encore analyse spectrale) repose à la fois sur l’organisation spatiale et sur les propriétés biophysiques très particulières des cellules mécanosensibles qui composent l’épithélium cochléaire, l’organe de Corti. Chaque position le long de la cochlée mature est en effet ajustée, du point de vue anatomique, mécanique et physiologique, pour permettre à une dizaine de cellules sensorielles (sur quelques milliers) de répondre à une fréquence sonore particulière, dite fréquence caractéristique. Notre objectif est de caractériser par une approche multi-échelle les mécanismes cellulaires et moléculaires qui façonnent la cochlée, au cours des premières étapes du développement, en un analyseur fréquentiel distribué spatialement. Le déchiffrage de ces mécanismes revêt un intérêt majeur aussi bien au plan fondamental qu’au plan de ses applications médicales potentielles.
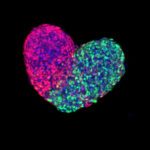
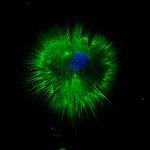
Ainsi, l’équipe travaille sur deux projets de recherche complémentaires, visant d’une part à comprendre les mécanismes cellulaires et moléculaires qui sous-tendent le développement de l’organe de Corti, et d’autre part, à générer, à partir de cellules souches, des organoïdes d’oreille interne récapitulant l’organisation spatiale de la cochlée in vivo ou en culture. De tels organoïdes fourniraient un outil très prometteur pour le développement de thérapies auditives, en permettant de modéliser certains troubles de l’audition de façon personnalisée et à faible coût.
Projets
Caractérisation des mécanismes cellulaires et moléculaires de l’établissement de l’organisation spatiale de l’organe auditif
Au cours du développement embryonnaire, l’épithélium cochléaire triple de longueur en 4 jours et acquiert une organisation en mosaïque, dans laquelle les cellules sensorielles auditives s’intercalent entre des cellules de soutien pour former des rangées précisément alignées. Les mécanismes moléculaires qui sous-tendent la mise en place de ces réarrangements cellulaires sont encore très mal compris. L’équipe a développé une approche intégrative combinant des outils génétiques avec des méthodes de microscopie multi-échelle, de bioinformatique, et d’intelligence artificielle, pour identifier les gènes et les voies de signalisations impliqués dans ce processus. En particulier, les chercheurs développent une méthode de transcriptomique spatiale permettant de corréler l’expression des gènes aux changements de forme des cellules. Cette méthode repose sur un ensemble de code-barres d’ADN permettant d’identifier, de manière unique, chaque position le long de l’épithélium cochléaire. Dans ce cadre, l’équipe a notamment mis au point un outil bioinformatique pour sélectionner des code-barres d’ADN robustes contre des erreurs de lecture de séquence. Dans ce but, les scientifiques ont utilisé les concepts issus de la théorie de l’information pour développer un nouvel algorithme permettant d’optimiser le choix de code-barres d’ADN. Ce code source a été rendu publique (10.18129/B9.bioc.DNABarcodeCompatibility) dans le dépôt Bioconductor et une interface web pour l’utilisation de cet outil (https://dnabarcodecompatibility.pasteur.fr) a été créé.
Organoid-on-chip : contrôle de l’organisation spatiale des organoïdes d’oreille interne
Le but de ce projet est de générer des organoïdes d’oreille interne qui puissent reproduire, in vitro, les premières étapes de formation de l’épithélium cochléaire. Plus précisément, l’objectif est de générer des organoïdes d’oreille interne dans un micro-environnement qui permette de contrôler la distribution spatiale de facteurs biochimiques diffusibles tels que des morphogènes, dont le rôle dans la mise en place des axes de l’épithélium cochléaire est essentiel. Les chercheurs combineront pour ce faire des outils avancés de microfluidique avec de l’imagerie à haut débit pour induire la différenciation et l’organisation de cellules souches embryonnaires en organoïdes cochléaires. Ce travail interdisciplinaire est en cours de réalisation en partenariat avec la plateforme de Biomatériel & microfluidique de l’Institut Pasteur, l’Institut Pasteur de Corée et l’université Nationale de Séoul.